Entresto® - synergetisch wirksames Kombinationspräparat bei Herzinsuffizienz hat EU-Zulassung
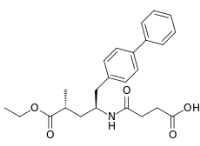
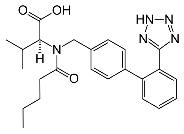
In einem beschleunigten Verfahren hatte die FDA eine Kombination aus Sacubitril (siehe Anm.) und Valsartan, einem Angiotensin-Rezeptor- und einem Neprilysin-Inhibitor (ARNI) bereits zugelassen. Seit November 2015 ist das Kombinationspräparat Entresto® auch in der EU zugelassen (1).
Pharmakalogie
Neprilysin ist für den Abbau natriuretischer Peptide verantwortlich. Durch seine Hemmung und dem damit verbundenen Anstieg natriuretischer Peptide sowie der AT1-Blockade lassen sich Synergieeffekte bei der Therapie der chronischen Herzinsuffizienz nutzen. Diese waren so überzeugend, dass vor knapp einem Jahr eine Vergleichsstudie von Sacubitril/Valsartan mit Enalapril (PARADIGM-HF) gestoppt werden musste, weil kardiovaskuläre Todesfälle und Klinikeinweisungen als Folge der Herzinsuffizienz in der Sacubitril/Valsartan-Gruppe um 20% niedriger als in der Enalapril-Gruppe waren(2)(3).
Anm.: Valsartan wirkt als AT1-Antagonist direkt am Angiotensinrezeptor. Damit soll im Gegensatz zu den ACE-Hemmern seltener der durch das Bradykinin ausgelöste Reizhusten auftreten (Bradykinin ist ein Peptid- und Gewebshormon der Kiningruppe das als vasoaktives blutgefäßveränderndes Oligopeptid ähnlich wie Histamin wirkt).
Entresto® wird üblicherweise mit anderen blutsenkenden Mitteln angewendet.
Hersteller: Novartis (Basel)
Quellen:
(1) http://www.swissinfo.ch/ger/novartis-erhaelt-eu-zulassung-fuer-herzmedikament-entresto/41797074
(3) http://www.pharma.us.novartis.com/product/pi/pdf/entresto.pdf
(AR)
(27.11.2015)