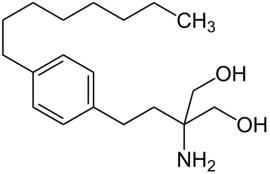
Neues zu Fingolimod (Gilenya®) – Multiple Sklerose
Der Pharmakonzern Novartis hat weitere Daten zur Wirksamkeit von Gilenya gegen Multiple Sklerose präsentiert: die Daten bestätigen, dass sich das Fortschreiten der Krankheit bei
Patienten mit schubförmig remittierenden Verlaufsformen aufhalten lässt, s.a. Neue Zürcher Zeitung v. 13.9.2014(1)
In der Entwicklungsphase III wurde seit 2006 geprüft, ob die in Phase II beobachteten Wirkungen über längere Zeiträume stabil bleiben, die Studien wiesen sowohl die Wirksamkeit von Fingolimod bezüglich der Schubrate als auch des Fortschreitens der Behinderung nach. Die Substanz ist inzwischen in Europa von der EMA unter dem Handelsnamen Gilenya® zugelassen.
Wirkungsmechanismus
Durch Fingolimod werden die Immunzellen nicht abgetötet oder an deren Vermehrung gehindert, die Substanz hemmt die Wanderung von Lymphozyten aus den lymphoiden Organen ins Blut. Dadurch wird die Zahl der entzündungsfördernden Lymphozyten gehemmt, diese können daher im Zentralnervensystem nicht mehr schädigend wirken (2).
Nach Einnahme von Fingolimod wird die Substanz durch das Enzym Sphingosin-Kinase-2 zu FTY720-Phosphat FTY720-P umgesetzt, welches dann die an die auf der Zelloberfläche vorhandenen Sphingosin-1-phosphat-(S1P)-Rezeptoren S1P1, S1P3, S1P4 u. S1P5 binden kann.
Für den Wirkungsmechanismus von FTY720-P ist vor allem der S1P1-Rezeptor auf T- und B-Lymphozyten wichtig. Diese Rezeptoren werden aus der Zellmembran ins Innere der Zelle verlagert und abgebaut. Durch diesen Abbau wird die S1P1 abhängige Auswanderung der Lymphozyten aus den Lymphknoten ins Blut und eine verminderte Einwanderung entzündungsfördernder Zellen in periphere Organe und ins Zentralnervensystem bewirkt.
Nebenwirkungen
Aufgrund seines Nebenwirkungsprofiles ist Fingolimod nicht als Basis- (oder auch Erstlinien) Therapie zugelassen. Es gilt zusammen mit Ntalizumab und Mitoxantron als Eskalationstherapie (oder auch Zweitlinientherapie) (2).
________________________
Anm.: Die Zulassung eines anderen MS-Präparats „Laquinimod“ (mit anderer chem. Struktur) wurde Anfang Januar 2014 von der EMA wegen beachtlicher Nebenwirkungen erneut abgelehnt(3), die Studien sollen jedoch weiter betrieben werden (Hersteller Active Biotech und Teva).
(AR)
(16.9.2014)
Quellen u.a.:
(2) amsel – Das Multiple Sklerose Portal :
http://www.amsel.de/multiple-sklerose-news/medizin/Gilenya-ausgezeichnet_4114
(3) http://www.dmsg.de/multiple-sklerose-news/index.php?kategorie=therapien&anr=4968